Närästys ja protonipumppulääkkeet
Seuraavat tiedot protonipummpulääkkeistä ja närästyksestä perustuvat alun perin A Midwestern Doctor -blogiin.

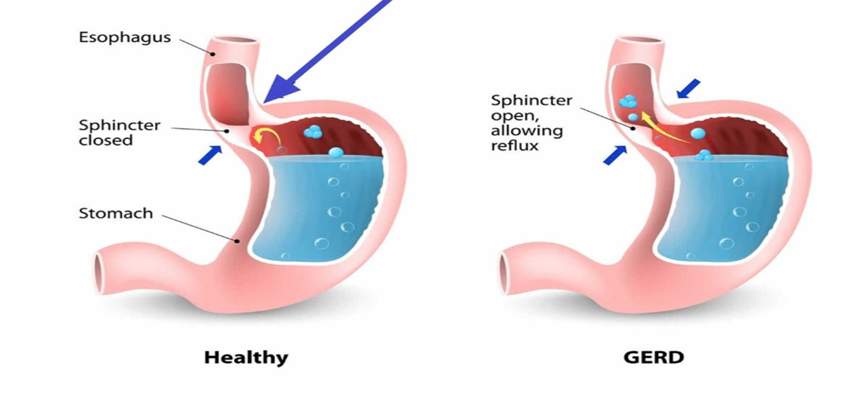
Refluksitaudin eli GERD:n (gastroesophageal reflux disease) oletetaan johtuvan aina mahahappojen liikatuotannosta. Refluksitaudin ilmaantuvuus kuitenkin lisääntyy iän myötä, vaikka mahahapon tuotanto vähenee luonnollisesti erityisesti 60 vuoden jälkeen. Mutta sen sijaan, että kysyttäisiin, voiko mahahapon puute aiheuttaa refluksiä vanhemmilla aikuisilla, oletuksena on edelleen liiallinen happamuuden muodostuminen. Mahahapon puute on paljon yleisempää kuin useimmat ymmärtävät, ja refluksitaudille on muitakin syitä.
- Palleatyrät lisäävät vatsanpainetta ja voivat mekaanisesti pakottaa refluksin.
- Jotkut lääkkeet, kuten keuhkoputkia laajentavat lääkkeet, kalsiumkanavasalpaajat ja opioidit, rentouttavat ruokatorven alempaa sulkijalihasta.
- Jotkut ruoat ärsyttävät jo tulehtunutta kudosta.
Protonipumppulääkkeitä (PPI, proton pump inhibitors) määrätään kuitenkin yleisimmin vanhemmille aikuisille – samalle väestölle, jolla on jo ennestään riski heikentyneeseen hapontuotantoon ja ravinteiden imeytymiseen. Lääketeollisuus haluaa meidän uskovan, että närästys johtuu liiasta haposta. Tuo oletus kuulostaa loogiselta. Happo polttaa. Refluksi polttaa. Tämä väärinkäsitys on pakottanut miljoonia ihmisiä lääkkeisiin, jotka saattavat pahentaa ongelmaa.
Mutta fysiologia ei oikeasti toimi niin, vaan mahalaukun tehtävänä on tuottaa suolahappoa. Ruokatorven alempi sulkijalihas, mahalaukun ja kurkun välissä oleva lihaksellinen läppä, on pH-herkkä. Se on suunniteltu sulkeutumaan tiiviisti, kun se havaitsee riittävästi happamuutta mahassa. Jos happotasot ovat liian alhaiset, signaali on heikko, läppä rentoutuu ja mahan sisältö nousee ylöspäin. Refluksi ei siis useinkaan ole seurausta liiallisesta hapon määrästä vaan ruokatorven alemman sulkijalihaksen sulkeutumisen epäonnistumisesta, koska mahalaukku ei ole tarpeeksi hapan laukaisemaan sulkeutumisrefleksiä.
Lääkeriippuvuus voidaan kuvata seuraavasti:
1 – Oire ilmenee.
2 – Lääke tukahduttaa sen nopeasti.
3 – Taustalla olevaan fysiologiaan ei puututa.
4 – Ajan myötä toissijaiset seuraukset kasaantuvat ja niitä hoidetaan lisälääkkeillä.
5 – Polyfarmasia laajenee.
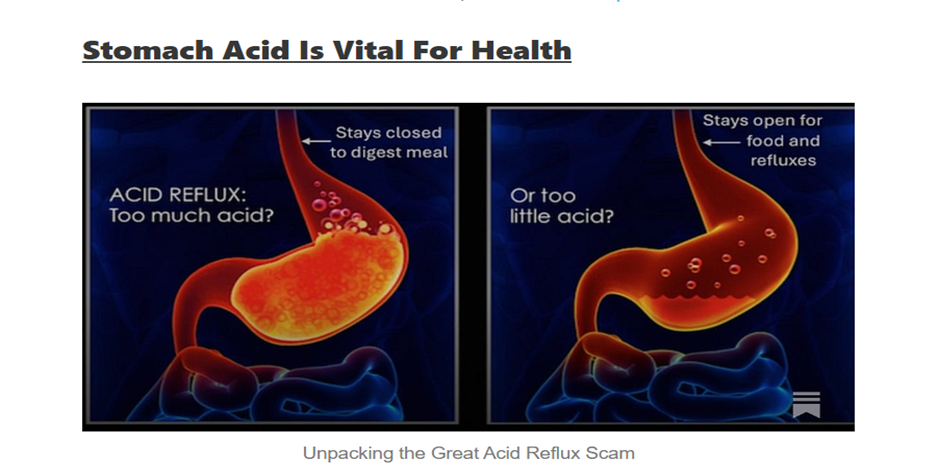
Tämä yksittäinen mekanismi kääntää koko tarinan päälaelleen, koska hapon tuoton esto poistaa juuri sen signaalin, jota vuodon korjaamiseen tarvitaan. Yksi PPI-annos voi tukahduttaa suurimman osan mahahapon tuotannosta koko päivän ajan.
PPI lääkkeet hyväksyttiin alun perin harvinaisiin sairauksiin, kuten Zollinger-Ellisonin oireyhtymään, todelliseen hapon ylituotantoon, johon lääkettä olisi pitänyt käyttää vain lyhytaikaisesti. Nyt närästykseen määrätään PPI lääkkeitä, joita potilaat käyttävät vuosia. Kun he lopettavat lääkkeiden käytön, refluksioireet palaavat, potilaat kokevat pahempia oireita ja aloittavat lääkityksen uudelleen.
Useimmat lääkärit eivät koskaan mittaa mahahappoa ja lähes kukaan ei tiedä, miten se palautetaan turvallisesti.
Mahahapon tuotanto vaatii energiaa.
Mahahappo ei ole evoluution virhe. Sen tuottaminen on itse asiassa aineenvaihdunnallisesti kallista. Mahahappoa tuottavat solut ovat täynnä mitokondrioita. Jos keho käyttää niin paljon energiaa suolahapon tuottamiseen syntymästä keski-ikään, se todennäköisesti palvelee kriittisiä toimintoja. Kun mitokondrioiden toiminta heikkenee, kuten usein tapahtuu kroonisessa sairaudessa, hapon tuotanto voi laskea. Autoimmuunihyökkäys happoa tuottavia soluja vastaan voi myös vähentää tuotantoa. H. pylori -infektio alussa nostaa suolahapon eritystä mahalaukussa mutta infektion kroonistuessa hapon tuotanto vähenee. Siksi H. pylori häädössä käytetään antibioottien lisäksi PPI lääkettä (esim. omepratsoli), mutta kuitenkin vain 10–14 vuorokautta.
Mahahappo on elintärkeää terveydelle
Mahahappoa tarvitaan monissa kriittisissä toiminnoissa, joita lääketieteen koulutuksessa tuskin korostetaan.
- Se aktivoi pepsiinin – entsyymin, joka aloittaa proteiinien pilkkomisen.
- Ilman riittävää happamuutta pitkät proteiiniketjut eivät hajoa kunnolla.
- Mahahappo on ensimmäinen puolustuslinja taudinaiheuttajia vastaan.
Aminohapot ovat raaka-aineita välittäjäaineille, lihasten korjaukselle, immuunisignaloinnille ja hormonien tuotannolle. Kun proteiineja ei ole täysin pilkottu, niiden fragmentit voivat kulkea suoliston läpi ja aiheuttaa immuunireaktioita. Ajan myötä tämä voi edistää ruoka-aineyliherkkyyksiä ja autoimmuunireaktioita. Tämä on yksi syy siihen, miksi mahahapon puutetta on toistuvasti havaittu autoimmuunisairauksia sairastavilla potilailla.
Mikroravinteiden imeytyminen on toinen usein vähemmälle huomiolle jäävä tekijä mahalaukun happamuuden muutosten yhteydessä.
Mahalaukun happamuudella on keskeinen rooli ravintoaineiden imeytymisessä sekä elimistön luonnollisessa puolustusjärjestelmässä. Happamuus auttaa vapauttamaan ravintoaineita ruoan rakenteista ja muuttaa ne kemialliseen muotoon, joka mahdollistaa niiden imeytymisen ohutsuolessa. Kun mahalaukun happamuus vähenee esimerkiksi happoa estävien lääkkeiden käytön seurauksena, myös tiettyjen mikroravinteiden imeytyminen voi heikentyä.
Riittävä happamuus on tärkeää erityisesti ravintoraudan liukenemiselle ja imeytymiselle, minkä vuoksi antasidien ja muiden happoa estävien lääkkeiden käyttö voi heikentää raudan imeytymistä [1]. Samoin kalsiumin imeytyminen voi heikentyä, ja kliinisissä tutkimuksissa on havaittu imeytymisen paranevan mahalaukun happamuuden palautuessa [2]. Myös magnesiumin, sinkin ja muiden mineraalien liukeneminen riippuu osittain mahalaukun happamuudesta, joka auttaa vapauttamaan mineraalit ravinnon rakenteista [3]. Lisäksi B12-vitamiinin imeytyminen edellyttää mahalaukun happoa, joka vapauttaa vitamiinin ravinnon proteiineista ennen sen sitoutumista sisäiseen tekijään [4]. Alhainen B12-vitamiinipitoisuus on yhdistetty neuropatiaan, väsymykseen, kognitiiviseen heikkenemiseen ja mielialahäiriöihin [4].
Mahalaukun happamuudella on myös tärkeä merkitys elimistön puolustusmekanismina, sillä se estää monien patogeenisten mikrobien selviytymistä ruoansulatuskanavassa. Happoa estävien lääkkeiden käyttöön on liitetty lisääntynyt alttius infektioille. Systemaattiset katsaukset ja meta-analyysit ovat osoittaneet, että protonipumpun estäjien käyttö lisää moninkertaisesti riskiä ruokaperäisiin infektioihin, kuten Salmonella– ja Campylobacter -infektioihin [5]. Samoin Clostridioides difficile -infektion riski on merkittävästi suurempi happoa estäviä lääkkeitä käyttävillä potilailla [6].
Sairaalaympäristössä happoa vähentävien lääkkeiden käyttö on yhdistetty myös hengitystieinfektioiden lisääntyneeseen riskiin. Mahahapon väheneminen voi lisätä bakteerien kolonisaatiota mahalaukussa ja ylähengitysteissä, mikä saattaa lisätä aspiraation kautta tapahtuvien infektioiden todennäköisyyttä. Havainnointitutkimuksissa happoa estävien lääkkeiden käyttö on liitetty suurempaan sairaalakeuhkokuumeen riskiin [7]. Tehohoitopotilailla tehdyissä tutkimuksissa mekaanisesti ventiloiduilla potilailla on raportoitu noin kaksinkertainen ventilaatioon liittyvän keuhkokuumeen riski happoa estävää lääkitystä käyttävillä potilailla, ja jopa noin 60 % suurempi kuolleisuus [8].
Pitkäaikaisen happoa estävän lääkityksen käyttöä on tutkittu laajoissa väestötutkimuksissa. Näissä tutkimuksissa protonipumpun estäjien käyttö on yhdistetty lisääntyneeseen kroonisen munuaissairauden riskiin, sydän- ja verisuonitapahtumiin sekä suurempaan kokonaiskuolleisuuteen [9]. Lisäksi meta-analyysit ovat raportoineet yhteyksiä dementiariskin kasvuun sekä mahalaukun syövän lisääntymiseen pitkäaikaiskäytössä [10]. Suurissa aineistoissa on kuvattu muun muassa noin 19 %:n kasvu kokonaiskuolleisuudessa, 28 % suurempi riski merkittäviin sydäntapahtumiin, 74 % kasvu vakavissa munuaissairauksissa sekä 142 % kasvu kuolleisuudessa munuaissairauden yhteydessä [9,10]. On kuitenkin tärkeää huomata, että suurin osa näistä tutkimuksista on havainnointitutkimuksia, jotka osoittavat tilastollisia yhteyksiä, mutta eivät todista suoraa syy-seuraussuhdetta.
Jo varhaisessa tutkimuksessa vuodelta 1931 seurattiin yli 200 astmaa sairastavaa lasta, joista yli 80 %:lla todettiin normaalia alhaisempi mahahapon eritys [8]. Laimennetun suolahapon antaminen paransi monien lasten tilaa merkittävästi, ja osa potilaista parani kokonaan. Samansuuntaisia havaintoja raportoitiin myös myöhemmissä 1900-luvun alkupuolen tutkimuksissa.
Laajoissa havainnointitutkimuksissa ja meta-analyyseissä happoa estävän lääkityksen käyttö on yhdistetty useisiin terveysriskeihin. Näihin kuuluvat keuhkokuumeen lisääntyminen, korkeampi kuolleisuus sepsispotilailla sekä kohonnut COVID-19 -kuolleisuus [7–10]. Iäkkäillä potilailla tehdyssä lääkityksen vähentämistutkimuksessa tarpeettomien lääkkeiden poistaminen vähensi yhdessä vuodessa kuolleisuutta 45 %:sta 21 %:iin [9].
Refluksitauti ei aina ilmene tyypillisenä närästyksenä. Osa potilaista kokee oireita ylähengitysteissä, kuten kroonista kurkkukipua, yskää, limaneritystä, paineen tunnetta korvissa tai poskiontelo-oireita. Tätä ilmiötä kutsutaan laryngofaryngeaaliseksi refluksiksi (LPR), ja sitä tavataan usein korva-, nenä- ja kurkkutautien klinikoilla [11]. Kaikki refluksit eivät siis aiheuta närästystä, ja niin sanottu “hiljainen refluksi” voi ilmetä monimuotoisina oireina ilman klassisia löydöksiä.
Tästä huolimatta monet happoa vähentävät lääkkeet ovat edelleen laajasti käytössä ja osin saatavilla ilman reseptiä. Tämä voi vahvistaa käsitystä niiden täydellisestä turvallisuudesta. Vaikka oireiden nopea lievittyminen on usein selvästi havaittavaa, pitkäaikaisia fysiologisia vaikutuksia voi olla vaikeampi tunnistaa. Refluksioireiden hoidossa voidaan käyttää muita lähestymistapoja, kuten ruokavalio- ja elämäntapamuutoksia, mekaanisesti vaikuttavia refluksivalmisteita sekä joidenkin tutkimusten mukaan tiettyjä kasviperäisiä valmisteita. Näiden menetelmien tehoa ja turvallisuutta tutkitaan edelleen.
Laimennettua suolahappoa annettaessa monien tila paranee dramaattisesti, ja jotkut paranevat kokonaan. Nämä havainnot ovat peräisin jo 1900-luvun alusta.
Referenssit
- Sharma VR, Brannon MA, Carloss EA. Effect of omeprazole on oral iron replacement in patients with iron deficiency anemia. South Med J. 2004;97(9):887–9.
- Recker RR. Calcium absorption and achlorhydria. N Engl J Med. 1985;313(2):70–3.
- Schinke T, Schilling AF, Baranowsky A, et al. Impaired gastric acidification negatively affects calcium homeostasis and bone mass. Nat Med. 2009;15(6):674–81.
- Allen LH. Causes of vitamin B12 and folate deficiency. Food Nutr Bull. 2008;29(2 Suppl):S20–34.
- Leonard J, Marshall JK, Moayyedi P. Systematic review of the risk of enteric infection in patients taking acid suppression. Am J Gastroenterol. 2007;102(9):2047–56.
- Janarthanan S, Ditah I, Adler DG, Ehrinpreis MN. Clostridium difficile–associated diarrhea and proton pump inhibitor therapy: a meta-analysis. Am J Gastroenterol. 2012;107(7):1001–10.
- Herzig SJ, Howell MD, Ngo LH, Marcantonio ER. Acid-suppressive medication use and the risk for hospital-acquired pneumonia. JAMA. 2009;301(20):2120–8.
- Cook DJ, Guyatt GH, Marshall JC, et al. A randomized trial of sucralfate vs antacids for the prevention of ventilator-associated pneumonia. N Engl J Med. 1998;338(12):791–7.
- Xie Y, Bowe B, Li T, Xian H, Yan Y, Al-Aly Z. Long-term kidney outcomes among users of proton pump inhibitors. J Am Soc Nephrol. 2016;27(10):3153–63.
- Hussain S, Singh A, Akhtar M, Najmi AK. Proton pump inhibitors’ use and risk of dementia: a meta-analysis. Pharmacol Rep. 2019;71(6):1040–8.
- Lechien JR, Saussez S, Schindler A, et al. Clinical outcomes of laryngopharyngeal reflux treatment: a systematic review. Otolaryngol Clin North Am. 2019;52(1):187–210.
Tamara Tuuminen, erikoislääkäri, dosentti
Helsingissä 18.maaliskuu, 2026






